攻克肿瘤前沿技术TILs免疫细胞疗法吉涛生物研发新型诱导和制备方法
TIL细胞疗法是指从患者自身的肿瘤组织中采集并分离出具有特异性识别肿瘤细胞抗原能力的T淋巴细胞,在体外通过白介素-2(IL-2)快速活化和扩增后再回输到患者体内, 最终实现对肿瘤的裂解和杀伤效果的一种细胞疗法。
TILs主要包括T细胞、巨噬细胞、NK细胞和树突细胞等,在TILs亚群中,起到正向调节免疫应答的免疫细胞包括CD4+Th1细胞、CD8+细胞毒性T细胞、NK细胞、巨噬细胞M1型和树突细胞DC1型等,可发挥很好的抗肿瘤细胞免疫应答。
另外,因TILs来自肿瘤组织,具有很强的肿瘤归巢特性,对肿瘤细胞具有良好的靶向作用,与其它免疫疗法(例如CAR-T、PD-1/PD-L1抗体)相比,TIL具有多靶点、肿瘤趋向和浸润能力强、副作用小等优势,是实体瘤治疗的理想选择,前景广阔。
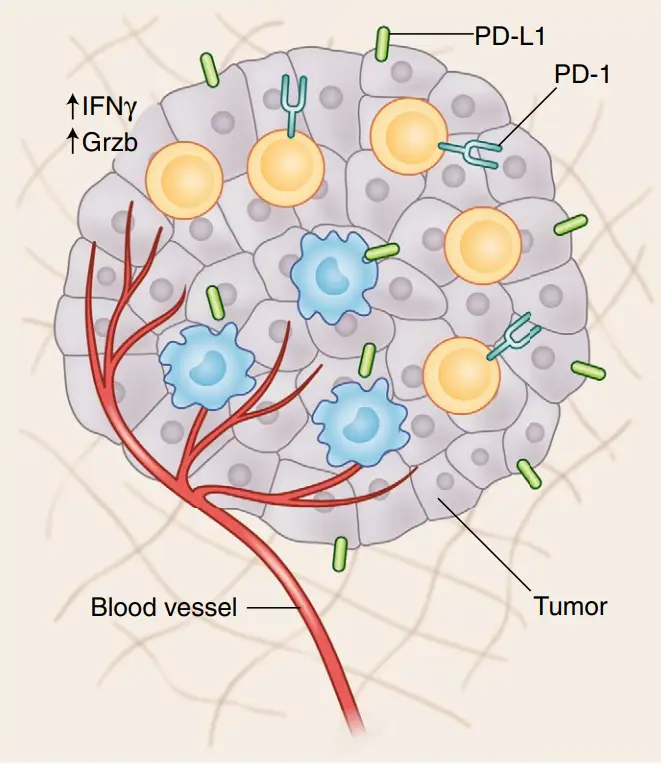
肿瘤组织中的TIL细胞(橙黄色)
01 细胞疗法的先驱——TIL疗法治疗实体瘤疗效显著
早在1982年,免疫学先驱Steven Rosenberg教授首次报导从多个小鼠肿瘤模型中分离出TIL[3];1985年,他又在《新英格兰医学杂志》(NEJM)报道了IL-2治疗转移性癌症的成果[4]。此时,人们已认识到IL-2可促进T细胞的增殖和功能,从肿瘤组织分离出TIL细胞,在体外经IL-2扩增后再输回患者体内进行肿瘤治疗成为可能。
1988年,NEJM发表了TIL疗法的最早临床数据,同样来自于Rosenberg团队。15例未接受过IL-2治疗的转移性黑色素瘤患者,经TIL治疗后达到了60%的客观缓解率(ORR)[5]。TIL疗法首次证实在实体瘤中具有疗效。随后,Rosenberg实验室的Patrick Hwu改进了TIL治疗方案,在接受TIL回输前,先使用化疗药物(环磷酰胺和氟达拉滨)清除患者体内的淋巴细胞,这一预处理方案显著延长了TIL疗法的维持时间,增强了抗肿瘤效果,并成为此后细胞疗法的标准操作。
2011年,Rosenberg确认了自体TIL细胞疗法可以在转移性黑色素瘤患者中介导持久的完全反应[6]。招募的93例患者中,20例患者肿瘤完全消退,达到完全缓解(CR),全部患者的3年和5年生存率分别为36%和29%,20例CR患者的3年和5年生存率分别为100%和93%。TIL疗法在晚期黑色素瘤中的数据在当时引起了极大的关注,实际上TIL疗法在多种癌症中均显示出良好的疗效。
TIL疗法在多种实体瘤中展现疗效
据吉涛生物创始人刘天津介绍,TIL疗法已在治疗宫颈癌、子宫内膜癌、黑色素瘤、胆管细胞癌、卵巢癌、胰腺癌等临床试验中取得令人可喜的疗效数据。TIL疗法是一个适应症覆盖面非常广的疗法,对于多种类型的实体肿瘤都能产生不错疗效。而吉涛生物新型的DC-TIL疗法将突破传统制备上的细胞数量,利用新型诱导技术和激活方式让战斗的细胞数值达到2400亿单位量。
02 TIL疗法治疗实体瘤——优势与挑战并存

传统TIL疗法流程
TIL疗法在实体瘤中取得的疗效基于其具有独特的优势:
03 技术创新对突破TIL疗法 技术壁垒极为重要
目前,TIL疗法已形成了一个标准治疗流程,其中注入的DC细胞-树突状细胞是近年来吉涛生物新兴的一种生物治疗恶性肿瘤的方法,已经越来越受到肿瘤专家的关注和认可。它主要是通过在体外短时间内诱导培养出大量的带有肿瘤抗原的树突状细胞,精确“瞄准”并杀伤癌细胞。不仅如此,它还能在患者体内诱发免疫记忆,使患者获得长期的抗癌效应。通过DC细胞和TIL细胞的双重结合,共培养时自体的DC细胞通过MHC分子递呈肿瘤抗原给TIL细胞,将会规模化扩增新生抗原TIL细胞(GT-001),简而言之即特异性杀伤肿瘤的有效细胞增多,更加精准化攻击。
新型研发技术DC-TIL主要包括以下几个步骤:

“我们的TIL细胞具有更高的肿瘤特异性”,据刘博介绍,当TIL细胞遇到肿瘤细胞刺激后,能更好的与肿瘤细胞反应,实现在体内的二次、三次扩增,并能够实现在患者体内不用额外输注就能很好的进行扩增。
目前,全球已上市多款细胞治疗产品,从销售情况来看并没有达到理想的预期。影响细胞疗法应用的主要因素有三个方面:一是疗效本身的不确定性,主要是能否治愈以及复发的挑战;二是价格因素,已上市细胞疗法都是定制化产品,高昂的生产成本导致药品售价过高;三是患者数量不确定,各种因素会影响到最终适合接受细胞疗法的人群数量。
事物的发展规律都是遵循前进性和曲折性必存。当Juno的JCAR015最早拿到FDA突破性疗法资格认定的时候,市场一致认为它会是第一个上市产品,但谁曾想CD28的强应答反而是成功路上的一个障碍。即便处于资本寒冬,只要脚踏实地坚持做自己认为对的事,稳扎稳打,市场会自动进行筛选。当一些追求热点,技术不太扎实的团队被排除在市场之外,留下具有更好技术含量、具有创新力和执行力的团队,对于整个行业的健康发展总体是有利的。在历史的洪流面前,任何可能都是存在的,毕竟在CAR-T细胞疗法领域我们国人已经为全球患者做出了创新药,相信在TIL疗法领域也一定会有收获!
参考文献:
[1]Chen X, Li P, Tian B and Kang X (2022) Serious adverse events and coping strategies of CAR-T cells in the treatment of malignant tumors. Front. Immunol. 13:1079181.
[2]Hernández-López A, Téllez-González MA, Mondragón-Terán P, Meneses-Acosta A. Chimeric Antigen Receptor-T Cells: A Pharmaceutical Scope. Front Pharmacol. 2021 Aug 20;12:720692.
[3]berlein TJ, Rosenstein M, Rosenberg SA. Regression of a disseminatedsyngeneic solid tumor by systemic transfer of lymphoid cells expanded ininterleukin 2. J Exp Med. 1982;156(2):385–97
[4]Rosenberg SA, et al. 1985.Observations on the systemic administration of autologous lymphokine-activatedkiller cells and recombinant interleukin-2 to patients with metastatic cancer.N Engl J Med 313(23):1485–1492.
相关阅读
-

攻克肿瘤前沿技术TILs免疫细胞疗法吉涛生物研发新型诱导和制备方法
TIL细胞疗法是指从患者自身的肿瘤组织中采集并分离出具有特异性识别肿瘤细胞抗原能力的T淋巴细胞,在体外通过白介素-2(IL-2)快速活化和扩增后再回输到患者体内...
-

整个知识付费的板块由内容、产品和用户组成;而若想做好一个知识付费产品也必须从这三个模块出发。 自2016年知识付费类产品爆发式增长后,2017年该领域的增长趋势依旧高歌猛进。...
-

在当今这个知识爆炸、信息瞬息万变的时代,我们如何为自己和孩子选择合适的教育方式,以应对未来社会的挑战呢?素养课作为一种新兴的教育理念,正逐渐受到...
-

《人民日报》:“每个人都有自己的人生节奏,你没必要非和别人比。江湖路远,山高水长,怕什么来不及,慌什么到不了。”
生活从来不会亏待每一个努力向上的人~...
-

四大旗舰(下)文字版四大旗舰的最终篇,我们聊聊系统、游戏以及续航的表现,交互、流畅性、玩游戏热不热、续航够不够持久等环节都和我们日常使用密切相关,属于智能手机的基础体验。...
-
“肉锥清网行动”迎2023年国际生物多样性日:为了众生的地球
生物多样性是地球上的生命之网。包括小到肉锥花属植物这样的物种,生物多样性不仅支撑着人类的现在和未来,而且其迅速减少正在威胁到自然界和人类的福祉。...
-

诗词天地,诗意生活倡导者。...
-

为了总结我们的经验和教训,需要将工作总结写好,工作结束后,整理好自己的思路可以让工作总结更有条理,以下是范文社小编精心为您推荐的镇卫生院疫情防控工作总结7篇,供大家参考。...
-

研究指出,TNF-α也可以由肿瘤相关微环境中的恶性细胞和免疫细胞产生,其作为内源性肿瘤启动子,通过产生炎症生态环境来促进恶性疾病的进展。...
-

春暖花开,气温多变,是传染病的高发时期,尤其是诺如病毒的高发时期。为快速有效地做好春季传染疾病的宣传工作,加强教师对诺如病毒的了解,以及正确采取预防措施,提高防控能力。近日...
-

1733年5月,建筑师约翰·格罗贝里去瑞典万林格博的采石场视察时,两名工人告诉他一个令人吃惊的消息。在开采位于地下3米多深的大块砂岩时...
发表评论
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件举报,一经查实,本站将立刻删除。

